每日經濟新聞 2022-07-01 14:37:38
每經記者|許立波 每經編輯|魏官紅
7月1日,《每日經濟新聞》記者從南京三迭紀醫藥科技有限公司(以下簡稱三迭紀)方面獲悉,公司首個3D打印藥物產品T19于近日獲得國家藥品監督管理局(NMPA)的藥物臨床試驗(IND)批準。該產品在中國按照2.2類改良型新藥進行注冊申報,是已知公開的首個在中國獲得IND批準的3D打印藥物產品。
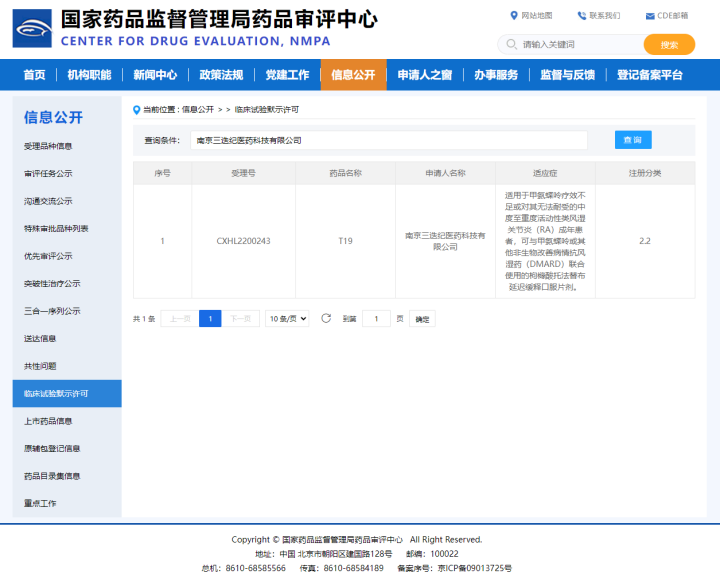
圖片來源:國家藥品監督管理局藥品審評中心官網
據三迭紀方面提供的書面材料介紹,T19是公司自主設計開發的具有全球知識產權的3D打印藥物。該產品根據時辰治療學原理,針對類風濕性關節炎癥狀的晝夜節律進行設計。患者睡前服用T19,血液中的藥物濃度在疼痛、關節僵硬及功能障礙等疾病癥狀最嚴重的早晨達峰,并維持其日間血藥濃度。
類風濕性關節炎在美國、中國等市場均有著巨大的臨床和市場需求,到2025年預計全球市場規模將達到307億美元(CAGR 4.5%)。根據中美臨床關鍵意見領袖(KOL)訪談意見,晨間癥狀仍然是困擾類風濕性關節炎患者的主要問題。
此前,T19在美國FDA通過505(b)(2)路徑進行注冊申報,于2021年獲得IND,是已知公開的全球第二款在美國FDA注冊申報的3D打印藥物產品。該產品接下來將分別在中國、美國開展臨床研究,并向NMPA和FDA遞交上市申請(NDA)。
封面圖片來源:攝圖網-500668961
如需轉載請與《每日經濟新聞》報社聯系。
未經《每日經濟新聞》報社授權,嚴禁轉載或鏡像,違者必究。
讀者熱線:4008890008
特別提醒:如果我們使用了您的圖片,請作者與本站聯系索取稿酬。如您不希望作品出現在本站,可聯系我們要求撤下您的作品。
歡迎關注每日經濟新聞APP
