每日經濟新聞 2022-06-14 22:01:29
◎又有一家疫苗企業叫停研發項目。6月13日,沃森生物公告稱,決定終止控股子公司上海澤潤研發的重組EV71疫苗的臨床研究工作。根據公司整體戰略,停止EV71疫苗研發后,上海澤潤將集中資源推進雙價HPV疫苗WHO PQ預認證、9價HPV疫苗研究、重組新冠疫苗海內外臨床研究等。
◎今年5月,萬泰生物稱公司的雙價HPV疫苗已獲得摩洛哥上市許可,這是國產雙價HPV疫苗獲得的首個境外上市許可。沃森生物內部人士則向記者表示,取得WHO PQ預認證是產品進入國際大宗市場的必要條件。
每經記者 陳星 每經編輯 魏官紅
繼三葉草生物(HK02197,股價3.39港元,市值39.35億港元)停掉3個在研疫苗項目后,沃森生物(SZ300142,股價44.41元,市值711.26億元)也對外宣布,控股子公司上海澤潤停止手足口疫苗研究。
6月13日晚,沃森生物發布公告稱,此次停止研發的重組腸道病毒71型病毒樣顆粒疫苗(畢赤酵母)(以下簡稱重組EV71疫苗)對于目前引起手足口病的主要病原體不具有預防作用,繼續研究的經濟效益和社會效益逐漸降低。此外,國內已有3家EV71滅活疫苗獲批上市,市場競爭將較為激烈。
上海澤潤也是沃森生物旗下負責HPV疫苗研發生產的子公司。目前,公司還有9價HPV疫苗以及重組新冠疫苗海內外臨床研究在進行中。沃森生物表示,上海澤潤將集中資源推動2價和9價HPV疫苗、重組新冠疫苗等相關工作。
又有一家疫苗企業叫停研發項目。
6月13日,沃森生物公告稱,決定終止控股子公司上海澤潤研發的重組EV71疫苗的臨床研究工作。
重組EV71疫苗主要用于預防因EV71病毒感染導致的手足口病。沃森生物稱,根據國內手足口病流行趨勢的演變情況,近年來我國手足口病發病率呈下降趨勢。在某些地方的特定時期內,柯薩奇病毒A16型(CA16)、A6型(CA6)和A10型(CA10)逐漸成為手足口病的主要致病毒株。而重組EV71疫苗對于上述病原體不具備預防作用,繼續研發該單價疫苗的經濟效益和社會效益將逐漸降低。
另外,國內已有3家EV71滅活疫苗獲批上市,尚有多家企業在研,公司預計該產品的未來市場競爭將較為激烈。
手足口病是一種由多種腸道病毒感染引起的急性腸道傳染病,其中EV71感染是導致手足口重癥和死亡病例的主要原因,可能導致嚴重的中樞神經系統疾病和其他并發癥。
對于手足口病,目前尚沒有特效治療藥物,因此盡早接種EV71疫苗對減少5歲及以下兒童手足口病重癥和死亡具有較大意義。國家衛健委頒布的《手足口病診療指南》和中國疾控中心的《腸道病毒71型滅活疫苗使用技術指南》中均提到,建議滿6月齡兒童盡早接種EV71疫苗,并在12月齡前完成全程接種,以便盡早發揮保護作用。
2016年后,全國報告的手足口病重癥大幅減少。2021年,全國報告手足口發病約135萬例,重癥和死亡病例數較少。在此情況下,EV71疫苗市場已有入局者。
《每日經濟新聞》記者注意到,目前國內外可接種的EV71疫苗均為國內廠商生產。其中包括VERO細胞工藝的EV71疫苗,生產廠家為武漢所、科興生物;另一種為人二倍體細胞工藝,生產廠商為中國醫學科學院醫學生物學研究所。
中國食品藥品檢定研究院數據顯示,2020年我國EV71疫苗批簽發量1551.35萬(支/瓶/袋),比上年減少333.7萬(支/瓶/袋)。其中,VERO細胞工藝批簽發量853.81萬,占比55%;人二倍體細胞工藝批簽發量697.54萬,占比45%。
6月14日,《每日經濟新聞》記者向沃森生物內部人士提出“停止EV71項目除了有市場需求和競爭原因外,是否也有公司研發投入收縮或謹慎原因”等問題,公司內部人士僅表示,“一切信息以公告為準”。
6月13日,沃森生物還在公告中稱,上海澤潤有多個產品陸續進入臨床研究關鍵時期。根據公司整體戰略,停止EV71疫苗研發后,上海澤潤將集中資源推進雙價HPV疫苗WHO PQ預認證、9價HPV疫苗研究、重組新冠疫苗海內外臨床研究等。
上海澤潤作為沃森生物研發生產HPV疫苗的主體,其最受外界關注的是HPV疫苗的研發進展。
據上海澤潤官網信息,公司研發項目中(截至去年5月),雙價HPV疫苗已經進入上市階段,9價HPV疫苗則已完成臨床I期,重組新型冠狀病毒疫苗(CHO細胞)臨床前研究已完成。此次終止的EV71疫苗也已完成臨床前研究。
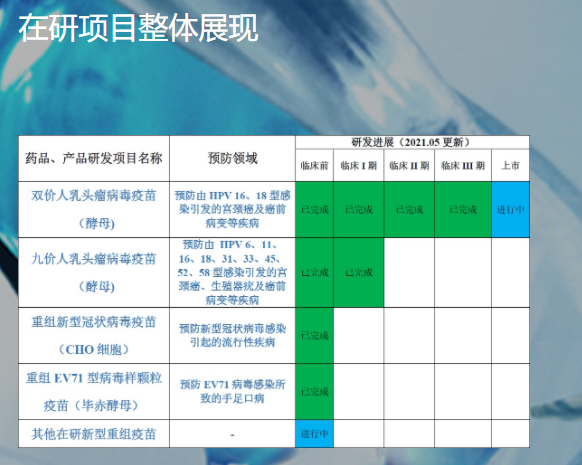
圖片來源:公司官網截圖
而截至今年5月,上海澤潤的雙價HPV疫苗已獲得國家藥監局簽發的《生物制品批簽發證明》,成為繼萬泰生物馨可寧之后上市的第二款國產雙價HPV疫苗。
但在目前國內HPV疫苗市場,9價HPV疫苗備受追捧且商業利潤較高,雙價HPV疫苗多用于地方政府或機構采購用于免疫計劃。今年5月,江蘇省公共資源交易中心曾發布一則群體性預防接種疫苗采購結果。該信息顯示,沃森生物子公司和萬泰生物子公司的雙價HPV疫苗中標,沃森生物的擬中標價為246元/支,萬泰生物的擬中標價為329元/支。在此次采購中,沃森生物以更低的價格搶占了更大的采購份額。
在國產雙價HPV疫苗存在價格競爭的背景下,雙價HPV疫苗“出海”也被視為擴大市場的重要途徑之一。
今年5月,萬泰生物稱公司的雙價HPV疫苗已獲得摩洛哥上市許可,這是國產雙價HPV疫苗獲得的首個境外上市許可。
而前述沃森生物內部人士表示,取得WHO PQ預認證是產品進入國際大宗市場的必要條件。
在九價HPV疫苗方面,沃森生物今年5月在投資者互動平臺上表示,九價HPV疫苗已經確定三期臨床試驗機構,臨床研究的相關準備工作完成后將正式啟動臨床試驗。
值得一提的是,沃森生物已經不是今年以來第一家停掉在研項目的疫苗企業。就在本月,三葉草生物公告稱,在完成內部科學、財務和戰略評估后,新冠候選疫苗SCB-2019的注冊申請是公司當前的首要任務。因此,公司決定將資源優先分配給新冠相關的產品及早期項目,減少對非新冠相關項目和新建基礎設施的投入,暫停對SCB-313(TRAIL-三聚體腫瘤產品)、SCB-808和SCB-420(Fc融合蛋白項目)的繼續投入。
與暫無產品上市銷售的三葉草生物相比,沃森生物已經有多個疫苗產品在售,擁有可持續的現金回血能力,但其仍需較高的研發支出。
2021年,沃森生物實現營業收入34.63億元,實現歸母凈利潤4.28億元,同期研發費用為6.21億元,達到近年新高。在公司3月21日披露的一份調研紀要中,沃森生物方面表示,去年超一半的研發費用投入到了新冠mRNA疫苗的臨床研究中。
封面圖片來源:攝圖網-500985021
如需轉載請與《每日經濟新聞》報社聯系。
未經《每日經濟新聞》報社授權,嚴禁轉載或鏡像,違者必究。
讀者熱線:4008890008
特別提醒:如果我們使用了您的圖片,請作者與本站聯系索取稿酬。如您不希望作品出現在本站,可聯系我們要求撤下您的作品。
歡迎關注每日經濟新聞APP
